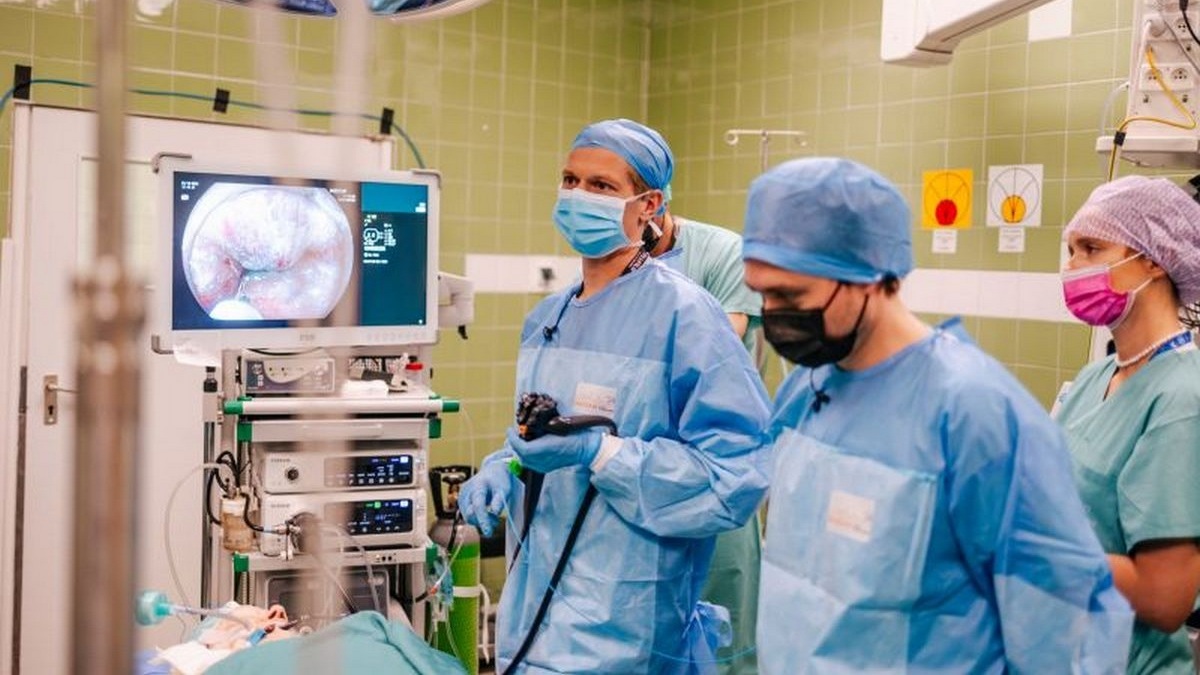
Dane z badania I fazy z wykorzystaniem bispecyficznego przeciwciała o aktywności anty-EGFR i anty-HER3 u pacjentów z zaawansowanym rakiem płaskonabłonkowym przełyku
W badaniu I fazy (NCT05262491) oceniono bezpieczeństwo oraz skuteczność koniugatu BL-B01D1 (złożonego z przeciwciała ukierunkowanego na EGFR oraz HER3 oraz inhibitora topoizomerazy I, Ed-04) u chorych z wcześniej leczonym zaawansowanym rakiem płaskonabłonkowym przełyku (esophageal squamous cell carcinoma – ESCC), w tym ustalenie zalecanej dawki do fazy 2 (recommended phase 2 dose – RP2D). Ustalono też zalecaną dawkę do fazy 2 (recommended phase 2 dose – RP2D).
Materiał przeznaczony wyłącznie dla pracowników służby zdrowia
Ten materiał jest dostępny dla zarejestrowanych użytkowników.
Zaloguj się
Szanowni użytkownicy,
część materiałów udostępnianych na naszym portalu jest przeznaczona
wyłącznie dla lekarzy.
Wynika to z regulacji prawnych, do których musimy się stosować.
Jeśli nie jesteś lekarzem, zachęcamy do korzystania z przygotowanych przez nas materiałów dostępnych w zakładce dla pacjentów.